Приготовление раствора методом сливания двух растворов
Задача №1:
Из двух растворов с концентрацией некоторого вещества 10 и 27 % необходимо приготовить 230 г раствора с концентрацией 17 %. Сколько грамм каждого из исходных растворов необходимо взять.
Дано:
ω1
= 10 %
ω2 = 27 %
ωx = 17 %
mx = 230
г
m1 - ?
m2 - ?
Решение:
Если раствор получают смешиванием двух других растворов, один из которых имеет большую концентрацию, а другой - меньшую, то массу исходных растворов можно определить, пользуясь правилом разбавления («правилом креста»), которое для растворов определенной процентной концентрации гласит: массы смешиваемых растворов обратно пропорциональны разностям процентных концентраций смешиваемых и получаемого растворов. Это правило выражают схемой:

При использовании этого правила следует помнить о том, что расчёт ведётся для масс растворов и если исходные данные в объёмах или необходимо найти объём, то необходимо использование справочных данных о плотностях растворов!!!
Применим правило для нашего случая:

Масса одной части:
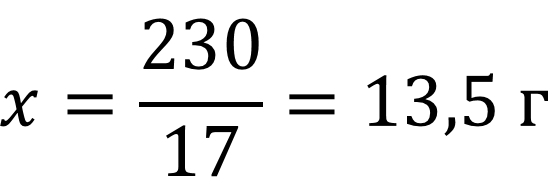
m1 = 10 * 13,5 = 135 г
m2 = 7 * 13,5 = 95 г
Для проверки рассчитаем сумму:
m1 + m2 = 135 + 95 = 230 г
Ответ: m1 = 135 г; m2 = 95 г.
Задача №2:
Смешали два раствора с массами по 100 г. Рассчитать конечную концентрацию, если исходные равны 11 и 30 %.
Дано:
ω1
= 11 %
ω2 = 30 %
m1,2 = 100 г
ωx -
?
Решение:
«Правило креста» - равносильно во всех направлениях и каждый элемент цепочки можно рассчитать, имея остальные данные, для данного случая:
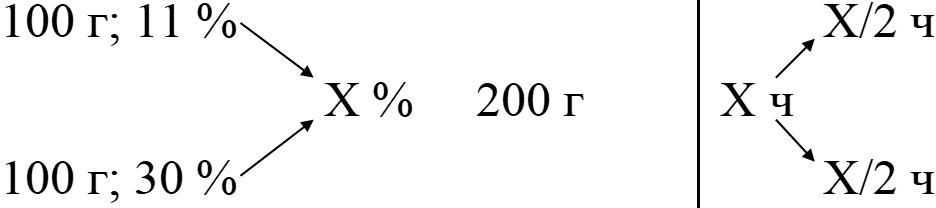
Соответственно:
ωx - ωменьш. = X/2
ωбольш. - ωх = X/2
Приравнивая:
ωx - ωменьш. = ωбольш. - ωх
Из полученного уравнения:
ωx - 11 = 30 - ωх
ωx = 20,5
Ответ: ωх = 20,5 %

