Расчёт количества осадителя
Следует помнить!
Для более полного выделения в осадок осаждаемого иона в раствор при осаждении вводят избыток осадителя по сравнению с рассчитанным по стехиометрии реакции. Если осадитель летучий, то рекомендуется использовать его 2–3-кратный избыток, если нелетучий – ограничиваются 1,5-кратным избытком.
Задача №1:
Какой объём 2,10 % - го раствора карбоната натрия (ρ = 1,020 г/мл) необходимо взять для полного осаждения кальция из навески образца (ωCa = 23, 5 %) массой 0,3716 г.
Дано:
mнав
= 0,3716 г
ωCa = 23, 5 %
ГФ – CaСO3
Определяемое
вещество – Са
ρр-ра = 1,020 г/мл
Vос-ля -
?
Решение:
Запишем схему превращения:
Ca ⇒ CaCO3
Рассчитаем необходимую массу раствора осадителя:
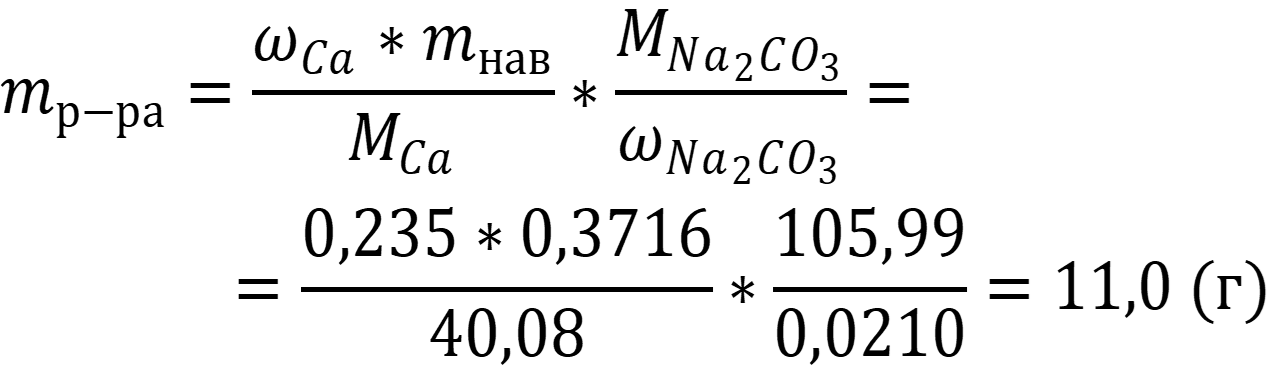
Рассчитаем объём раствора осадителя, необходимого для полного осаждения кальция:
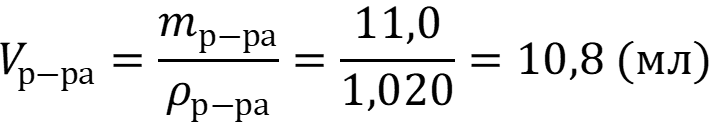
Раствор карбоната натрия не является летучим и согласно правилу берётся полуторакратный избыток для полного осаждения определяемого иона.
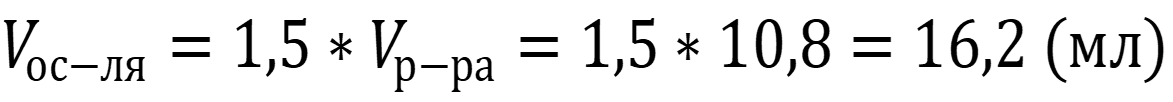
Ответ: Vос-ля = 16,2 мл.
Задача №2:
Какой объём 0,1 М раствора соляной кислоты (ρ = 1,000 г/мл) необходимо взять для полного осаждения ионов серебра из раствора содержащего 70 мг нитрата серебра.
Дано:
mAgNO3
= 0,007 г
CHCl = 0,1 M
ГФ – AgCl
Определяемое вещество
– Ag
ρр-ра = 1,000 г/мл
Vос-ля - ?
Решение:
Рассчитаем количество ионов серебра в растворе с учётом полной диссоциации соли:
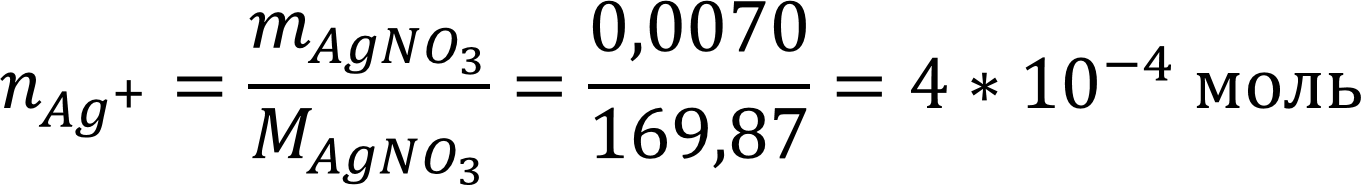
Рассчитаем объём раствора осадителя, необходимого для полного осаждения кальция, с учётом реакции один к одному:
Ag+ + Cl- ⇒ AgCl
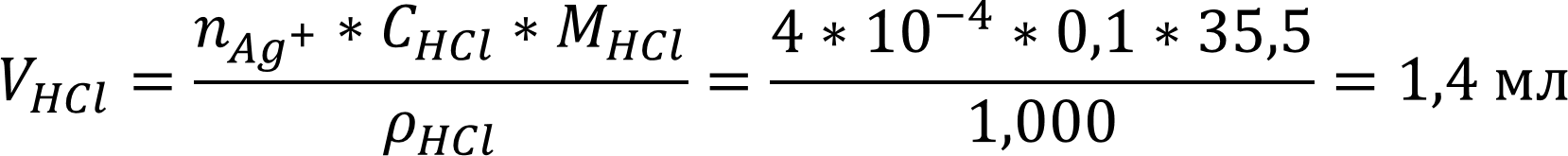
Раствор соляной кислоты является летучим и согласно правилу берётся двукратный избыток для полного осаждения определяемого иона:
Vос-ля = 1,4 * 2 = 2,8 (мл)
Ответ: Vос-ля = 2,8 мл.

